CMAC發布 單臂和開放標簽臨床試驗的實操與考量——以工程和技術研究試驗發展為例
近年來,隨著藥物研發的加速和監管環境的靈活化,單臂和開放標簽臨床試驗在工程和技術研究試驗發展中扮演著越來越重要的角色。CMAC(Clinical Trials and Medical Affairs Community)近期發布了相關指南,重點關注這兩種試驗設計的實操細節和關鍵考量因素。本文將基于CMAC的指導,結合實際案例,系統探討單臂和開放標簽試驗的應用場景、優勢、局限以及實施中的注意事項。
一、單臂試驗的實操與考量
單臂試驗(Single-Arm Trial)是一種沒有平行對照組的臨床試驗設計,常用于罕見病、突破性療法或晚期腫瘤藥物的研發。其實操要點包括:
- 患者選擇:需嚴格定義入組標準,確保人群同質性。
- 終點設定:通常采用客觀緩解率(ORR)等替代終點,需與監管機構提前溝通。
- 數據分析:依賴歷史數據或外部對照,但需注意偏倚風險。
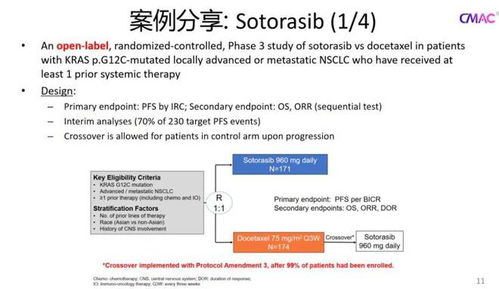
考量方面,單臂試驗的優勢在于縮短研發周期和降低成本,但局限在于無法完全控制混雜因素,可能影響結果的可推廣性。實際案例中,某腫瘤藥物通過單臂試驗基于ORR數據獲得加速批準,但后續需進行確證性試驗。
二、開放標簽試驗的實操與考量
開放標簽試驗(Open-Label Trial)中,研究者和受試者均知曉治療分配,常用于長期安全性評估或患者報告結局(PRO)的研究。實操關鍵點包括:
- 盲法缺失的補償:通過獨立終點評審委員會減少評估偏倚。
- 患者依從性管理:開放設計可能影響行為,需加強監測和教育。
- 數據收集:強調真實世界數據整合,提高外部有效性。
考量中,開放標簽試驗便于實施和患者招募,但可能引入期望偏倚。案例顯示,一項慢性病治療試驗通過開放標簽設計成功收集了長期安全數據,但需通過統計方法調整偏倚。
三、工程和技術研究試驗發展中的應用
在工程和技術研究試驗發展領域,單臂和開放標簽試驗常用于醫療器械、數字健康工具或新型治療技術的評估。例如,某智能醫療設備采用單臂試驗驗證其有效性,通過與歷史性能比較獲得監管認可;另一項開放標簽試驗評估了患者對遠程監測技術的接受度,為產品優化提供依據。這些試驗強調快速迭代和實用性,但需平衡創新與證據強度。
四、總結與建議
CMAC的指南強調了單臂和開放標簽試驗在特定場景下的價值,尤其是加速工程和技術創新。實操中,研究者應注重方案設計、偏倚控制和監管溝通。未來,隨著真實世界證據和自適應設計的融合,這些試驗模式有望進一步優化。建議行業加強培訓,并參考實際案例,以提升試驗質量和效率。
如若轉載,請注明出處:http://m.dj7uug.cn/product/20.html
更新時間:2026-03-01 18:20:58